李黎专访细胞外RNA开创者张辰宇:体内自组装药物递送平台,是RNAi疗法的未来 | 未来百科018期
03.30.2022
|
嘉程资本Next Capital
|
新闻动态

撰文 | 李黎
编辑 | 王聪
一手访谈,带你了解细胞外RNA世界,和这一领域的开创者张辰宇教授团队的系列研究突破,以及当前的临床转化。
关于未来百科:未来百科(Next Biotech)是嘉程资本携手生物世界联合发起的访谈100位中美优秀Biotech科学家的项目,旨在真实访谈开启未来的100位Biotech的科学家,探讨生物科技/生命科学领域的全球最新技术和商业趋势,展现华人生物科技科学家在该领域的贡献与成就,剖析创新的生物科技公司的最佳商业实践,共同推进生物科技/生命科学行业在中国的茁壮成长。
第018期未来百科的访谈嘉宾,是南京大学生命科学学院院长张辰宇教授,以下为文章正文。
作为细胞外RNA(exRNA)研究领域的开创者,现任南京大学生命科学学院院长张辰宇教授的实验室在过去十多年来,一直致力于细胞外miRNA的研究,并取得了一系列颠覆性和原创性发现,也因此被誉为“国际细胞外RNA研究第一人”。
2008年,张辰宇团队在 Cell Research 发表关于miRNA可在人类和动物的血清和血浆中稳定存在的原创发现,这篇论文也是中国学者被引用数量最多的论文之一。这一发现,开创了细胞外RNA研究的新领域,也成为所有血清miRNA生物标志物研究的基础。
此后,张辰宇实验室陆续发现了植物来源的miRNA对人体的跨界调控、分泌miRNA通讯交流系统、中药金银花通过MIR2911发挥抗病毒作用、细胞外囊泡(EV)可作为小RNA递送载体等等。
2021年,张辰宇实验室开发出了第三代RNAi药物体内递送平台,这一递送平台可在异质动态体内环境中诱导了可控和可预测的siRNA自组装和递送,并能够精确调控基因表达,提供了一种可行的策略来克服RNAi体内治疗应用的最重要障碍,让RNAi疗法治疗从癌症到代谢疾病成为可能。
2022年张辰宇教授创立的艾码生物融资数千万元,专注于小RNA核酸药物研发。近日,生物世界与嘉程资本携手推出的《未来百科》访谈了张辰宇教授,共同探讨了细胞外RNA(exRNA)领域的发展趋势。
未来百科:首先请张教授介绍一下自己是怎么进入生命科学领域的,以及一直以来的成长之路。
张辰宇:我从小是在哈工大的院子里长大的,但10岁前是在老家扬州被爷爷奶奶带大的,我的家庭一直在从事教育工作,到我和我弟弟这一代,已经是第五代了。爷爷奶奶是学理工的,父亲母亲也是,所以他们也一直希望我能学理工,通信之类的,将来接他们的班。但我出生的时候,正赶上文革,父亲那时候正在蹲地下室接受强制劳动批斗。我的爷爷奶奶虽然都是学理工的,但那个时代受过高等教育的人,比较传统,对中国传统文学、历史有比较深入的学习,跟着他们我受到了很多文学熏陶,所以我一度是想学文的。但在哈工大的环境下,学文似乎是一件不能被接受的事情。我15岁的时候考大学,那时候心智也不成熟,也没考好,但我坚决否定了父母当时让我再考一次的建议,而去学了医。一开始,其实我对医学也没什么感觉,直到大三时涉及了临床,才开始对医学真正感兴趣。
毕业后,我先后去了日本德岛大学和美国哈佛大学读博和做博士后。留学后,我更加喜欢了生命科学,或者说生物医学和基础医学的研究了。一直以来,我的求学经历都非常顺利,这让我觉得自己是一个幸运的天选之人,这也让我有着比其他人更强的使命感,这种使命感不仅是我要去揭示自然规律,还要把我做的研究转化并应用到临床,去解决现在还没被满足的疾病治疗,甚至是生命从哪里来到哪里去的哲学问题。
实际上,20多年来,我的实验室一直有一个座右铭:“做配享冷猪肉的研究,让世界和我们接轨”。在过去文人学问高、人品好,死后是要进文庙,和孔夫子一起享受后人祭祀的冷猪肉。只有我们长年累月苦学苦研、甘于寂寞,坐得冷板凳,引领科学发展,泽被当下和后世的人类、社会和自然界,才吃得冷猪肉。
未来百科:在美国学习和工作多年,当时你是怎么考虑回国发展的呢?
张辰宇:在我有了自己独立实验室后,我就已经想要回国发展了,这和我的家庭背景以及自己的性格有很大关系。我的父亲是在哈工大做研究,我当时出国留学时就想着学成回国。而且,那时候在哈佛已经有了自己的独立实验室,但20年后会怎样?其实基本也就看得到,所以我也不甘心就这样了。当时正好南京大学蒋树声校长到哈佛大学邀请我对面实验室的一位南大校友回国建生命科学,他推荐了我,于是我当时作为兼职教授入职了南京大学。
在当时,我已经确定了要回国发展,不过具体什么时候回,去哪里,还没有明确的目标。那时候,我和我的爱人在美国发展的比较顺利,她从MIT毕业后去了当时的通信巨头朗讯公司工作,我们还在波士顿有6套独立出租的房子。在2002年的时候,刚好有了这样的一个机会,南京大学生命科学学院院长换届,于是我全职回国,加入南京大学生命科学学院,并出任院长。所以我也很感激我的爱人,在当时的情况下支持我回国。
在回国加入南京大学前,我还咨询了三个人的意见——我的父亲(中国第一个航天学院的院长和工程院院士)、原哈工大校长杨士勤教授、原协和医科大学校长巴德年院士。结果是他们三位都从不同的角度,坚决支持和鼓励我回国发展,看好我的性格和能力能在国内做好,能为国家发展做一些事。
未来百科:留学时候你的研究方向是能量代谢,再到后来的细胞外RNA,这些科研方向是怎么选择和转换的?
张辰宇:刚去留学的时候其实我还不确定自己喜欢哪个方面,当时的导师是做内分泌代谢的,当时主要做的就是开发新方法来测定内分泌相关的一些激素,当时所受的这些严格训练为10多年后发现细胞外RNA作为生物标志物(Biomarker)奠定了基础,这或许就是冥冥之中的安排吧。博士毕业后,我申请了哈佛大学的博士后,在哈佛期间,我做的也是代谢研究,主要是糖尿病。当时哈佛的博后老板只比我大八岁,当时我们俩关系处的就像兄弟一样,他是一个特别热爱研究,而且单纯又有胸怀的人。很快我因为线粒体解偶联蛋白2(UCP2)在糖尿病中的作用的一系列研究而在哈佛有了自己独立的实验室。当时我的经费只够配备一个技术员和一个博士后,动物实验所需的大量经费都是由当时的博后老板提供的。
我当时做的是线粒体相关的能量代谢研究,尤其是UCP2、UCP3,但是我们发现了一个很奇怪的现象,就是在心肌细胞和骨骼肌细胞里面有UCP2的mRNA,但却检测不到对应的蛋白。在2003年的时候,MIT的一个博士后发现miRNA在哺乳动物细胞中同样起作用,能够阻止mRNA向蛋白质的翻译,而不影响mRNA本身。他在论文还没正式发表的时候,就来哈佛做了报告,我当时立刻意识到,这很可能解释了我们的困惑。我当时在美国的实验室的研究方向是固定的,难以开展新研究,而当时在南京大学的实验室已经成立了,我就打电话让当时硕士二年级学生陈熹(现在是南京大学生科院教授,生物化学系主任)验证一下,是不是骨骼肌中的miRNA抑制了UCP2的表达,这也是当时国内最早做miRNA研究的。也就是我当时提出了这个规划,陈熹建立起了我们实验室的miRNA研究系统。
在细胞内,miRNA的作用说得好听些是精确调节,起辅助作用,换而言之,细胞内miRNA的作用既非必要,也不充分。但是细胞中存在着这么一大类miRNA,不应该既非必要也不充分的作用,那么只有一个原因,就是我们对miRNA的认知还不够。大约在2005年的时候,我意识到了这一点,于是就决定从进化的时间轴上,研究miRNA在原始动物细胞里面不可或缺的作用,另一个是拓展空间轴上,检测miRNA能否在细胞外稳定存在,并发挥不可或缺的生物学功能。
在核酸的研究,特别RNA的研究,前面有两个阶段,一个是中心法则,另外一个发现了具有和蛋白质一样的特定生物学功能的RNA,包括各种小RNA。但之前经典生物化学概念认为核酸只能稳定的存在于细胞内并发挥生物学功能,在细胞外只能以无生物学功能的降解碎片存在,因为细胞外RNA水解酶无处不在。
之后,我和原华大基因CEO王俊合作,在文昌鱼中对miRNA进行深度测序,这也是世界首个对miRNA的深度测序。这些研究我们后来在血清、血浆中发现稳定存在的miRNA,以及人体对食物中miRNA的吸收起到了决定性作用。
接下来就是2007年,我安排陈熹鉴定miRNA是否能够在血清血浆等体内的细胞外环境存在。但有趣的是,我当时安排这个实验后,过了两个多星期陈熹还没开始做,他当时还跟实验室其他师弟师妹说,自己是经过严格的生物学和生物技术训练的南大毕业生,不会浪费时间来验证老板的错误想法。两周后我在实验室堵住他,让他立刻开始去做。在做完第一个实验后,他连续三天三夜没睡,把miRNA在血清和血浆中的验证实验做完了。
2008年我们在 Cell Research 发表关于miRNA可在人类和动物的血清和血浆中稳定存在的原创发现,我们使用深度测序对人血清中的miRNA谱进行了表征,并确定了独特的血清miRNA模式,从而将癌症和糖尿病患者与健康受试者区分开。这些发现表明,体内的细胞外环境中是由miRNA稳定存在的,而且特定的血清miRNA谱可作为疾病诊断标志物。这一原创发现,开创了细胞外RNA研究的新领域,也成为所有血清miRNA生物标志物研究的基础。谷歌学术显示这篇论文目前已被引用超过5000次,是中国学者被引用数量最多的论文(之一)。
此后,我们进一步揭示了miRNA能在细胞外环境中稳定存在的原因,并在2011年发现了食物来源的miRNA可以被人体吸收,并调控人体基因,也就是所谓的miRNA的跨界调控。这项研究在当时也引发了很大的轰动。
之后在2021年,我们揭示了胃部SIDT1蛋白介导食物来源的miRNA吸收的分子机制,为“哺乳动物能吸收并利用食物来源的miRNA这一近十年来细胞外RNA研究领域中最具突破性和争议性的发现之一”提供了有力证据,从而结束了这个领域长达10年的争论。
到现在,我们已经认识到,miRNA几乎参与了所有的生命现象和生命过程的调控,细胞外RNA还能够执行蛋白质无法行使的不可或缺的生物学功能。
未来百科:你们之前开发了基于血清miRNA的体外诊断产品,这些产品或试剂盒现在有应用吗?
张辰宇:这项研究当时发在了国产期刊 Cell Research 上,我们当时发现了miRNA可在人类和动物的血清和血浆中稳定存在,这是一个原创发现,开创了细胞外RNA研究的新领域,也成为所有血清miRNA生物标志物研究的基础。
基于这项研究,我们在2015年,开发的国际上首个针对miRNA标志物的胰腺癌诊断试剂盒获得国家批准,对早期胰腺癌的检测准确率达87.6%。其中正在复旦大学附属华山医院推广的应用,去年上半年做的双盲检测,准确率达到了100%。
此外,我们现在还在做基于miRNA标志物的精神疾病的检测诊断,因为精神疾病如精神分裂症、抑郁症等等,没有明确的客观指标,我们发现了一些生物标志物,这样就能更准确地进行筛查了。
未来百科:你们之前发现金银花是通过其编码的MIR2911来发挥抗病毒作用,这能够用来开发口服的小RNA药物,来预防和治疗病毒感染吗?
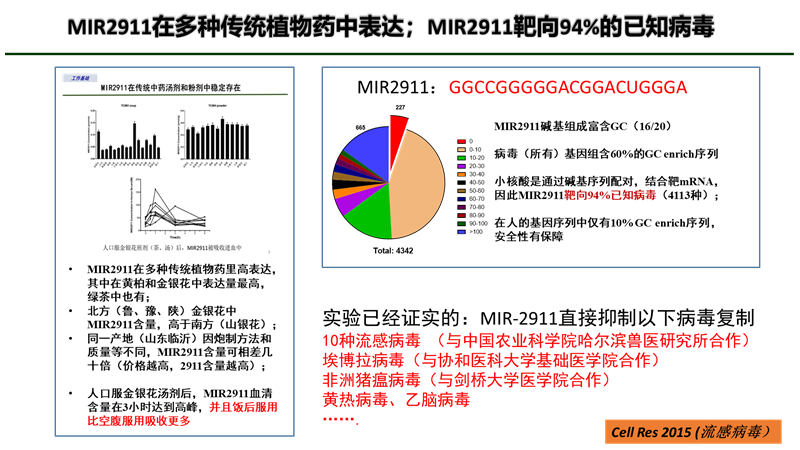
张辰宇:我们当时发现,金银花在作为中药汤剂时,即使经过长时间煮沸,仍然存在富集的完整序列的MIR2911,这是由于其序列中GC含量高,在高温下仍能保持稳定。
在体外和体内试验中,MIR2911能够靶向多种流感病毒基因,抑制病毒复制,减轻病毒感染引起的体重减轻,并降低了小鼠死亡率。
该研究还提供了第一个证据,证明植物miRNA可能是中药中的活性成分,并确定了首个有助于抑制病毒感染的植物miRNA。
而在2020年8月,我们在 Cell Research 发表的论文,揭示了哺乳动物胃中的SIDT1蛋白介导食物miRNA的吸收,进而使其在动物体内发挥生物学功能。这项研究解析了SIDT1介导食物miRNA吸收的分子机制,为“哺乳动物能吸收并利用食物来源的miRNA——近十年来细胞外RNA研究领域中最具突破性和争议性的发现之一”提供了有力证据,也结束了这个领域长达10年的争论。
这些研究让我们发现了胃的新功能和核酸吸收的新途径——胃直接吸收食物中的miRNA,为基于小RNA的治疗提供了新的策略,也为基于RNA的药物开发提供了潜在方向。
未来百科:当时是如何发现胃对miRNA的吸收是通过SIDT1蛋白介导的呢?
张辰宇:我们在发现食物来源的miRNA能够被胃吸收后,肯定要弄清楚吸收的具体机制。当时我们首先猜测,这种对miRNA的吸收可能与RNA结合蛋白有关,当时已经开始逐一敲除所有已知的RNA结合蛋白来进行研究。当时我们大课题组的董磊(现在是南京大学生科院教授,副院长),在文献中看到SIDT1在细胞膜上表达,而且能够转运双链RNA。
有了这个线索后,我们利用SIDT1基因敲除小鼠,首先发现SIDT1在胃的顶细胞膜上表达,而不在十二指肠和小肠表达,这个发现首先提示了SIDT1有可能在消化道介导miRNA的吸收,第二却是颠覆了传统的消化生理学的概念,即胃只能吸收水、酒精和几个小分子,大部分的食物成分是在小肠被降解吸收。进而证实了SIDT1介导了胃对食物来源的miRNA的吸收。而且这种介导作用依赖于胃部的低pH环境,这也从进化的角度解释了为什么动物消化系统能完整地吸收利用外源miRNA,因为胃部始终保持低pH的酸性环境,在这种环境下RNA酶基本没有活性,保证了外源miRNA在胃里的稳定性。
未来百科:基于这些发现,能否开发一些用来口服递送miRNA、siRNA或者mRNA的药物及疫苗呢?
张辰宇:外泌体是不行的,实际上在胃里头不能被吸收,到了小肠以后被降解,这是第一个。然后现在miRNA口服本身,我们发现的现在还没有解释机理的,但是也被大家用来攻击的,植物里面的自然产生的miRNA在吃完吸收了以后,能够达到体内工作浓度所需要的量,是人工合成的同种miRNA的几千分之一。所以需要进一步研究吸收机制,从而才能开发些用来口服递送miRNA、siRNA药物。至于mRNA疫苗等,或许需要开发运送载体吧,SIDT1只能介导小RNA的吸收,对mRNA等大片段RNA没有作用。
未来百科:你们实验室在2021年3月发表论文,开发了第三代RNAi药物体内递送平台,它的原理是什么,又是如何想到这种方式的呢?
张辰宇:我们在2010年左右的时候就发现了外泌体或其他细胞外囊泡中携带的miRNA能够靶向调控基因表达,之后我们还探索了使用外泌体作为RNAi递送载体进行疾病治疗的研究。但利用培养细胞并提取外泌体的方式,效率并不高。
但我们发现,内源分泌的miRNA可以在极低浓度下发挥功能。于是我们开始计划将表达特定siRNA的质粒注射到肝脏中,重编程宿主肝脏,并以肝脏细胞为底盘,指导siRNA的合成和自组装成分泌性外泌体,并通过循环外泌体促进siRNA的体内递送。也就是利用人体细胞本身作为细胞工厂,产生分泌型、药用小RNA。
我们还使用这种第三代RNAi药物体内递送平台对肺癌(靶向EGFR/KRAS)、胶质母细胞瘤(靶向EGFR/TNC)、肥胖症(靶向PTP1B)和亨廷顿症(靶向mHTT),证实了这种体内自组装siRNA策略能够有效沉默这些关键致病基因,并产生显著治疗效果。
这也是我们创立的专注于小RNA核酸药物研发的艾码生物(ExoRNA Bio)的核心技术,我们将基于这一第三代RNAi药物体内递送平台开发用于脑神经性疾病核酸药物和抗超级菌、抗病毒感染性疾病核酸药物,并在将来为未满足的临床需求带来创新性的治疗方案。
未来百科:这种药物体内递送平台,能否用来开发预防性或治疗疫苗呢?
张辰宇:实际上我们已经在做基于外泌体的自组装疫苗了,在去年7月份已经获得了初步结果,通过这种体内药物递送平台,在体内细胞自组装表达抗原的外泌体,在一定程度上,能够解决现在mRNA疫苗的卡脖子问题,也就是递送问题。
未来百科:刚才讲到的第三代RNAi药物体内递送平台,有进行胶质母细胞瘤的治疗研究,这是如何突破血脑屏障,实现向脑细胞的递送呢?
张辰宇:我们是通过在质粒上添加了融合蛋白,也就是一个来自狂犬病毒(RVG)的十二肽,正是它通过与神经细胞表面的乙酰胆碱受体结合介导狂犬病毒进入神经细胞。因此,当这个十二肽表达在外泌体膜上,就能够介导外泌体通过血脑屏障,从而将治疗性siRNA递送到大脑细胞。
未来百科:这种第三代RNAi药物体内递送平台,也属于当下很火的合成生物学范畴,你觉得现在合成生物学距离真正的应用还有哪些障碍?
张辰宇:合成生物学的方向很大,我没有资格贸然点评,现阶段大多数合成生物学的研究是对细菌的改造,让他们来产生一些有用的产物。但我们这个是直接将合成生物学应用到人体和动物体内,在体内自组装成治疗性药物,算是合成物学的一个实际临床应用的突破吧。
未来百科:你是基于怎样的考虑成立了艾玛生物,艾玛生物现阶段的研发管线有哪些?
张辰宇:最大的契机实际上是mRNA疫苗,让大家看到了RNA药物的巨大潜力。然后是我们的这项持续了10年的第三代RNAi药物体内递送平台的研究发表了。此外,《生物世界》也功不可没,对我们这些成果系统的科学的报道,让很多人关注到了这些成果,并找到了我们。
我们现在在做的研发管线可以分为以下几类,对难治性实体瘤的治疗,例如胰腺癌等;对中枢神经系统疾病的治疗,例如亨廷顿症、帕金森病、脑胶质瘤;以及金银花中MIR2911的广谱抗病毒研究,这包括对新冠病毒的治疗作用。
未来百科:这种体内自组装的小RNA疗法,作为一种创新的递送和治疗方式,在安全性验证上的周期是否会更长,是否需要花费更多的时间来获得临床批准?
张辰宇:这是个非常好的问题,总体时间上未必长,因为整个实验的过程不长,在解决了递送系统的情况下,小RNA药物比抗体药的研发周期快得多,在实验室做完动物实验后,就可以直接进入到CMC和IND阶段,在IND的时候,我们只需要多做一些更可靠的大型动物实验,例如非人灵长类动物实验。而且我们选择的研发管线,大多是目前缺少有效治疗方法的疾病,能够相对容易地进行研究者发起的临床试验(IIT)。
未来百科:这一第三代RNAi技术具有很好的临床转化和应用前景,那么你们实验室接下来还会继续之前的miRNA跨界调控的研究吗?
张辰宇:这两个方向我们都将继续研究,比如我们提出了RNA因子(RNAkines)和RNA免疫(RNA Immunity)的新概念,它们在内稳态和免疫中的作用都需要进一步研究。对于miRNA的跨界调控,我们现在还要证明它是人体所需的碳水化合物、脂肪、蛋白质、维生素、水和矿物质之外的第七种营养素,证明它是物种间共进化和适应的媒介,证明它介导了代际遗传,以及证明它是传统中药中发挥作用的物质等等。还有我们正在做的转基因的表达抗乙肝病毒RNAi生菜、番茄等抗病毒食品等等,这些都是我们在miRNA跨界调控领域还要做的研究。
未来百科:你目前有重点关注哪些生物医药领域的发展?
张辰宇:生物医药领域很大,很难做出全局性的看法。我们之前常说,21世纪是生物的世纪,在我看来,核酸生物学已经开始让这句话变成现实了。
未来百科:你看好哪些国内外的生物医药领域创业公司?
张辰宇:对于产业界来说,我只是一个新来者,我对这些生物医药创业公司都是抱着学习和崇敬的态度。像Moderna、BioNTech这些前沿mRNA技术公司,他们说是开拓者,也是先驱,但同时也需要持续创新和发展,否则先驱一不小心就变成了先烈。
未来百科:你在 Nature 发表过一篇题为:NanjingSchool: Extracellular microRNA mediates co-evolution between species (南京学派:细胞外miRNA介导物种之间的共进化)的Highlight文章,我们应该如何理解“南京学派”这个称呼?
张辰宇:这实际上是在逐步研究的过程中慢慢形成的一个概念。生命存在的最基本的条件是对特定时空的适应,进化是适应的手段和方法。我们发现小RNA为代表的核酸,能够在物种间、代际间稳定存在,还能携带特定功能信息并发挥直接作用,在此基础上,我们提出了细胞外小RNA介导了物种间的共进化和适应的理论,这一理论也可以叫做学派,我们将其称之为南京学派(Nanjing School)。就像对量子力学的创立和发展做出重要贡献的哥本哈根学派,南京学派也是一个基于研究理论而存在的概念。


嘉程资本Next Capital是一家专注科技领域的早期投资基金,我们极度信仰科技驱动的行业创新,希望成为创新者的第一笔钱,与极具潜力的未来商业领袖共同开启创新的未来。
我们的投资领域涵盖新消费、新技术、新医疗。投资案例包括熊猫速汇、多抓鱼、十荟团、拉面说、店匠、bosie、熊猫星厨、核桃编程、橄榄枝健康等多家创业公司的天使轮或早期阶段。
嘉程资本旗下的创投服务平台「嘉程创业流水席」,致力于为科技互联网创业者和行业人士提供深度链接和一手行业信息,迄今已服务数万名创业者,汇聚了数百个创业者社群,有近千位企业家与行业专家在嘉程创业流水席分享过行业观点。
嘉程资本创始合伙人李黎是知名天使投资人,曾主导投资过乐信(纳斯达克代码:LX)、团车(纳斯达克代码:TC)、老虎证券(纳斯达克代码:TIGR)、牛股王、蜜芽、辣妈帮、PingCAP、易订货、彩贝壳、鹿客、Krazybee等明星公司的天使轮。
嘉程资本是创业者思考的伙伴,成长的伙伴。
嘉程资本
握手未来商业领袖
BP 请发送至 BP@jiachengcap.com
微信ID:NextCap2017